2015, Vol 13, No 2
Ocena funkcji układu moczowego oraz komfortu życia kobiet po skojarzonym leczeniu raka endometrium
Marcin Opławski, Radosław Kosobudzki, Michał Kwiatkowski, Zbigniew Kojs
Curr Gynecol Oncol 2015, 13 (2), p. 78–84
DOI: 10.15557/CGO.2015.0009
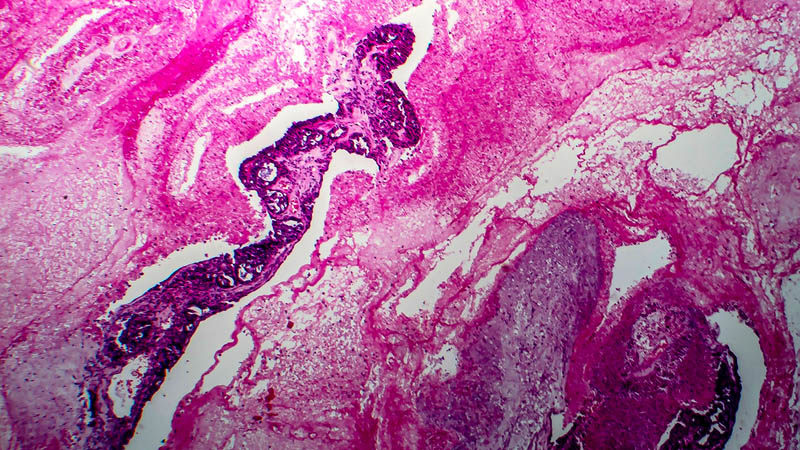
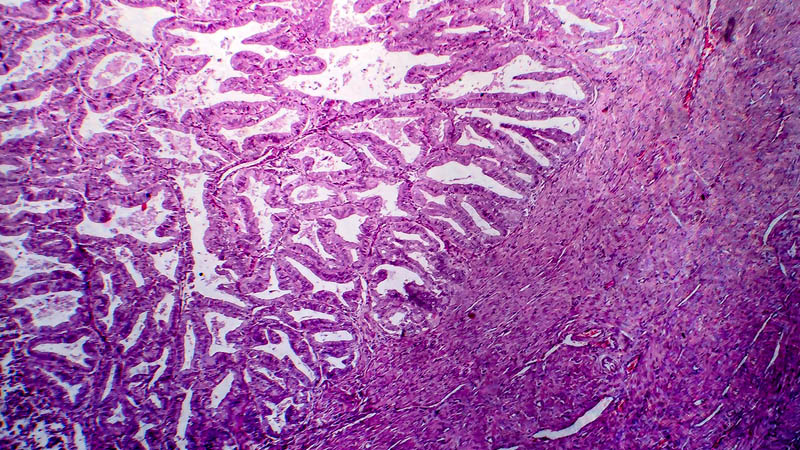
Histopatologia raków jajnika współistniejących z endometriozą
Elżbieta Stasienko, Magdalena Wiśniewska, Krzysztof Kamecki, Joanna Skręt-Magierło, Marcin Opławski, Anna Brożyna, Magdalena Maleńczyk, Krzysztof Koper, Krzysztof Roszkowski
Curr Gynecol Oncol 2015, 13 (2), p. 85–92
DOI: 10.15557/CGO.2015.0010
Rokownicze znaczenie stanu ogólnego WHO u chorych na raka szyjki macicy
Agnieszka Żółciak-Siwińska, Joanna Jońska-Gmyrek, Leszek Gmyrek
Curr Gynecol Oncol 2015, 13 (2), p. 93–98
DOI: 10.15557/CGO.2015.0011
Rozległość limfadenektomii w raku endometrium oraz jej wpływ na utratę krwi i czas trwania zabiegu
Marcin Opławski, Tomasz Bieda, Marcin Zarawski, Zbigniew Kojs
Curr Gynecol Oncol 2015, 13 (2), p. 99–105
DOI: 10.15557/CGO.2015.0012
Jakie są perspektywy biopsji węzła chłonnego wartowniczego?
Wojciech M. Wysocki, Jerzy W. Mituś, Jan Gawełko, Zbigniew Kojs
Curr Gynecol Oncol 2015, 13 (2), p. 106–112
DOI: 10.15557/CGO.2015.0013
Guzy gonadalne jajnika ze szczególnym uwzględnieniem guza szkliwiejącego. Znaczenie wczesnej diagnostyki zmian jajnika
Magdalena Pisarska-Krawczyk, Grażyna Jarząbek-Bielecka, Anna Grętkiewicz-Tomczyk, Małgorzata Mizgier, Witold Kędzia
Curr Gynecol Oncol 2015, 13 (2), p. 113–122
DOI: 10.15557/CGO.2015.0014
Właściwości i kliniczne możliwości zastosowania ludzkich komórek nabłonka owodni (HAEC)
Arkadiusz Gawryluk, Bartłomiej Noszczyk
Curr Gynecol Oncol 2015, 13 (2), p. 123–135
DOI: 10.15557/CGO.2015.0015